1 minute de lecture
Zerlasiran, encore un nouvel antiLp(a) en développement
En direct du congrès de l'AHA 2024 - Chicago
Publié le jeudi 21 novembre 2024
Étude ALPACAR-360 – D’après la présentation de Steven E. Nissen
L’étude évaluait l’efficacité et tolérance d’un nouvel antiLp(a).
Messages clés
- zerlasiran nouveau petit ARN interférent antiLp(a)
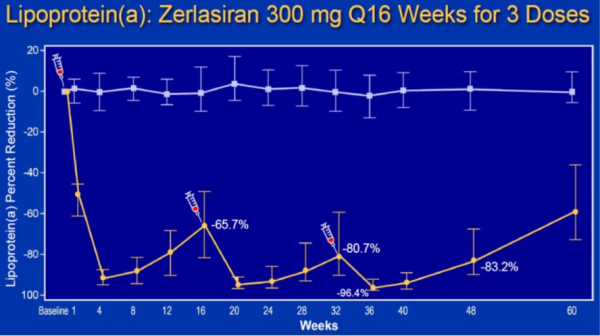
- réduction d’au moins 80% du taux circulant de Lp(a) à 60 semaines
- injections tous les 4 à 6 mois par voie sous-cutanée
- bonne tolérance
- efficacité et tolérance d’un nouvel antiLp(a)
Méthodologie et résultats
Étude phase II.
Patients à haut risque de maladie athérosclérotique présentant un taux de Lp(a) A à 125 nmol/L.
Étude de dose durée d’activité avec une dose de zerlasiran 300 mg tous les 4 mois et un autre bras une de dose de Zerlasiran 300 mg tous les 6 mois contre deux bras placebo à 4 et 6 mois.
Critères de jugement : taux de Lp(a , ApoB à 60 semaines.
Résultat principal : baisse d’au moins 80% de la Lp(a) dans les deux bras.
Résultats critères secondaires : baisse du LDLc de près de 30% et apoB de 12%.
Sécurité si essai thérapeutique : bonne tolérance clinique et biologique, pas de différence avec le placebo.
Figure 1
Conclusion
Efficacité confirmée d’un nouvel antiLp(a) de type ARN interférent avec possibilité d’injection tous les 4 à 6 mois.
Dans la même thématique
Articles les plus lus

Efficacité et sécurité d’emploi de l’obicetrapib, un nouvel inhibiteur de la CETP
Publié le 21 novembre 2024
La muvalaplin : nouvel inhibiteur de la lp(a) par voie orale
Publié le jeudi 21 novembre 2024
Effet du tirzepatide dans l’insuffisance cardiaque à fraction d‘éjection préservée chez le sujet obèse
Publié le mardi 19 novembre 2024
Place des ARM en post-infarctus en absence de défaillance cardiaque
Publié le mardi 19 novembre 2024
Prise en charge agressive des facteurs de risque dans la fibrillation atriale (ARREST-AF)
Publié le mercredi 20 novembre 2024