4 minutes de lecture
Étude POPular PAUSE TAVI : interrompre ou poursuivre les anticoagulants pendant un TAVI ?
Publié le lundi 2 septembre 2024
En direct du congrès de l'ESC 2024
D’après la présentation de Dirk Jan Van Ginkel, Pays-Bas « POPular PAUSE TAVI - Continuation or interruption of oral anticoagulation during TAVI : International, randomized, open-label, noninferiority trial »
Messages clés
- La stratégie concernant la gestion péri-interventionnelle des anticoagulants oraux lors d’un TAVI reste débattue.
- POPular PAUSE TAVI est un essai contrôlé, randomisé, de non-infériorité, en ouvert, ayant inclus des patients allant bénéficier d’un TAVI, randomisés pour interrompre ou poursuivre les AO en pré-TAVI.
- Dans cet essai, la non-infériorité de la stratégie de poursuite des anticoagulants n’a pas été démontrée, en comparaison avec la stratégie d’interruption, sur le critère de jugement principal (décès cardiovasculaires, accidents vasculaires cérébraux de toutes causes, infarctus du myocarde, complication vasculaire majeure et saignement majeur à 30 jours post-TAVI), avec un taux de saignement plus élevé dans le groupe poursuite des AO.
- Les résultats de cette étude ne suggèrent pas un bénéfice à la poursuite des anticoagulants pour la réalisation d’un TAVI.
Introduction
Parmi les patients adressés pour TAVI, 35% sont sous anticoagulant oral (AO), principalement prescrits pour de la fibrillation atriale (FA) (1). Cette population est particulièrement fragile, poly-comorbide, à risque ischémique/thrombo-embolique et hémorragique. La stratégie concernant la gestion péri-TAVI des AO n’est pas clairement définie dans la littérature. Les recommandations proposent de les interrompre (2,3) mais chez les patients en FA, le bénéfice n’est pas clairement défini. Certaines études observationnelles suggèrent la possibilité de les poursuivre avec un bénéfice sur les évènements thrombo-emboliques comme les accidents vasculaires cérébraux (AVC), sans majoration du risque hémorragique (4,5).
L’objectif de cette étude était d’explorer l’efficacité et la sécurité de la poursuite des AO lors d’un TAVI.
Méthodologie et résultats
Il s’agit d’un essai contrôlé, randomisé, multicentrique, en ouvert, de non infériorité (marge de non-infériorité de 4%, taux d’évènements attendu de 17,5% dans le groupe témoin), qui a inclus des patients sous AO qui allaient bénéficier d’un TAVI, randomisés en 1:1 pour interrompre (groupe témoin) ou poursuivre les AO (groupe expérimental) en pré-TAVI. La population était stratifiée sur le type d’AO : AVK ou AOD. L’arrêt des AO se faisait selon un protocole établi : entre 5 et 2 jours pré-procédure selon le type d’anticoagulant et la fonction rénale, et sans relai. Leur reprise était prévue à partie du lendemain de la procédure. Les patients à haut risque cardio-embolique (porteurs de prothèse valvulaire mécanique, de thrombus intra-cardiaque, de maladie thrombo-embolique veineuse < 3 mois, d’accident ischémique transitoire (AIT) ou d’accident vasculaire cérébral (AVC) avec fibrillation atriale (FA) < 6 mois) étaient exclus. Le critère de jugement principal était le composite des décès cardiovasculaires, accidents vasculaires cérébraux, infarctus du myocarde, complication vasculaire majeure et saignement majeur à 30 jours post-TAVI. Les critères de jugement secondaires étaient les éléments du critère de jugement principal pris individuellement.
Au total, 869 patients ont été inclus dans 22 centres européens, 858 ont été analysés dans l’analyse en intention de traitée modifiée (âge moyen 81 ans, 65% d’hommes, score CHA2DS2-VASC moyen de 4,5): 431 dans le groupe expérimental et 427 dans le groupe témoin. Leurs principaux antécédents comportaient : FA (> 95%), AVC ischémique (10%) et insuffisance rénale chronique (50%). 82% étaient sous AOD et 18% sous AVK ; 12% avaient en plus un traitement angiagrégant plaquettaire. Près de 99% des procédures ont été réalisées par voie fémorale, avec anticoagulation curative per-procédure par bolus d’HNF IV et réversion par protamine.
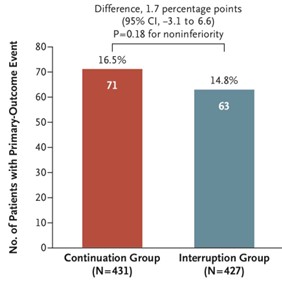
L’analyse du critère de jugement principal est négative pour la non-infériorité, avec 71 (16.5%) évènements dans le groupe poursuite et 63 (14,8%) dans le groupe interruption des AO (différence de risque de 1,7%, IC 95% : −3.1 to 6.6, p=0,18 pour la non infériorité) (Figure 1).
Figure 1 : bar chart du critère de jugement principal
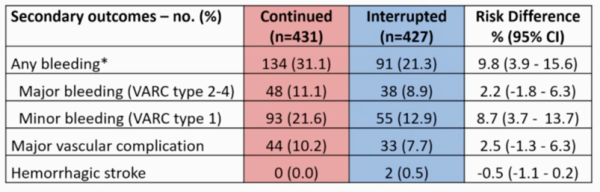
L’analyse des critères de jugement secondaires retrouve 8% d’évènements cardio-emboliques, sans différence significative entre les 2 groupes ; mais un nombre d’événements hémorragiques plus important dans le groupe expérimental (31,1% vs. 21,3%, différence de risque : 9,8%, IC 95% : 3,9-15,6) drivé par les saignements mineurs (VARC type 1), avec une tendance non significative sur les saignements majeurs (VARC 2-4). 91% des évènements hémorragiques étaient péri-procéduraux (Tableau 1).
Tableau 1 : évènements hémorragiques survenus dans les 30 jours post-TAVI
L’analyse en sous-groupes ne retrouve pas de différence selon le type d’AO mais une tendance en faveur du groupe témoin si score CHADS-VASC ≥ 5 et score de fragilité d’Edmonton > 5.
Conclusion
Dans l’essai POPular PAUSE TAVI, chez les patients sous AO bénéficiant d’un TAVI, la poursuite des anticoagulants n’était pas non-inférieure à leur interruption sur le critère composite associant les évènements cardio-vasculaires majeurs et les événements hémorragiques. Le nombre d’événements hémorragiques était plus important en l’absence d’interruption des AO.
Pour aller plus loin
Le design de l’étude en non-infériorité et le critère de jugement principal choisi peuvent être discutés. En effet, le composite des événements cardiovasculaires et hémorragiques ne permet pas de mettre clairement en miroir l’éventuel bénéfice de la stratégie sur les événements thrombotiques avec le risque de perte sur les événements hémorragiques.
D’autres stratégies pourront être testées, notamment une interruption plus brève des AO (24h pré-procédure par exemple alors que la durée d’arrêt dans cette étude était de 2 à 5 jours avant le TAVI selon l’anticoagulant et la fonction rénale).
Références
1. Capodanno D, Collet JP, Dangas G, Montalescot G, Ten Berg JM, Windecker S, et al. Antithrombotic Therapy After Transcatheter Aortic Valve Replacement. JACC Cardiovasc Interv. 2021 Aug 9;14(15):1688–703.
2. Douketis JD, Spyropoulos AC, Murad MH, Arcelus JI, Dager WE, Dunn AS, et al. Perioperative Management of Antithrombotic Therapy: An American College of Chest Physicians Clinical Practice Guideline. Chest. 2022 Nov;162(5):e207–43.
3. Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2018 Apr 21;39(16):1330–93.
4. Brinkert M, Mangner N, Moriyama N, Keller LS, Hagemeyer D, Crusius L, et al. Safety and Efficacy of Transcatheter Aortic Valve Replacement With Continuation of Vitamin K Antagonists or Direct Oral Anticoagulants. JACC Cardiovasc Interv. 2021 Jan 25;14(2):135–44.
5. Brinkert M, Keller LS, Moriyama N, Cuculi F, Bossard M, Lehnick D, et al. Safety and Efficacy of Transcatheter Aortic Valve Replacement With Continuation of Oral Anticoagulation. J Am Coll Cardiol. 2019 Apr 23;73(15):2004–5.
Dans la même thématique
Articles les plus lus

Études BedMed & BedMed Frail : à quel moment prendre son traitement antihypertenseur ?
Publié le 31 août 2024
Recommandations ESC 2024 pour la prise en charge des maladies aortiques et artérielles périphériques : les messages à retenir
Publié le jeudi 5 septembre 2024