16 minutes de lecture
ESC 2024 : les messages clés des recommandations de la maladie vasculaire périphérique et des pathologies aortiques
En direct du congrès de l'ESC 2024
Publié le mardi 3 septembre 2024
Les messages clés des guidelines 2024
- Les maladies vasculaires périphériques et aortiques sont des pathologies fréquentes. Souvent asymptomatique et sous-diagnostiquée, leur présence se révèle être un marqueur de risque cardiovasculaire puissant associé à une augmentation de la mortalité toutes causes et à un risque d’événement cardiovasculaire majoré par 4 à 5.
- Son dépistage est recommandé par le calcul de l’index cheville-biceps et la mesure de pression artérielle aux 4 membres.
- En l’absence de symptômes, la revascularisation systématique d’une maladie vasculaire périphérique n’est pas recommandée (grade III). Les stratégies de revascularisation apparaissent en 2nde ligne en cas de persistance de symptômes malgré l’optimisation du traitement médical.
- L’activité physique fait partie intégrante de la prise en charge non invasive de l’artériopathie périphérique symptomatique à travers des programmes supervisés et stéréotypés
- Les scénarios d’ischémie aiguë et d’ischémie chronique menaçante requièrent un diagnostic et une évaluation précoce pour la réalisation d’un geste de revascularisation rapide.
- La chirurgie des anévrysmes de l’aorte ascendante, que la valve aortique soit bicuspide ou tricuspide, est dorénavant envisagée au seuil >52 mm (grade IIa) chez des patients à faible risque opératoire dans des centres experts.
- Ce seuil d’intervention peut être abaissé à partir d’une dilatation ³50 mm (grade IIb), chez des patients à faible risque opératoire, en présence notamment : d’un anévrysme localisé à la racine aortique (phénotype racine), d’un âge < 50 ans, d’une taille < 1.69 m, d’une longueur aortique > 11 cm ou d‘une progression de l’anévrysme ³ 3 mm/an. En l’absence, un contrôle à 6 mois est recommandé.
- Bien que la meilleure méthode de mesure des diamètres aortiques soit encore débattue, la stratégie de référence reste la mesure du diamètre aortique telediastolique bord interne à bord interne. Les variantes morphologiques de la racine doivent être décrites telle qu’une asymétrie >5 mm suggérant une pathologie aortique héritable ou la présence d’une bicuspidie aortique.
- La surveillance d’un anévrysme de l’aorte thoraco-abdominale >40 mm repose sur la réalisation d’une imagerie annuelle. En présence d’une valve aortique bicuspide et en l’absence d’évolutivité au contrôle à 1 an, cette dernière peut être renouvelée dans un délai de 2 à 3 ans.
- Devant la présence d’un syndrome aortique aigu probable, le diagnostic de dissection fait dorénavant appel à l’algorithme ADD-RS basé sur : la présence d’un terrain à risque, la caractérisation des symptômes et la présence d’anomalie clinique évocatrice à l’examen clinique. Une stratégie rule-in / rule-out mentionnant le dosage des D-Dimères est précisée.
- La réalisation d’un dépistage génétique est guidée par une enquête familiale rigoureuse ³3 générations, recherchant des antécédent d’anévrysme de l’aorte thoracique, de mort subite inexpliquée <60 ans, d’anévrysme périphérique ou intracrânien en présence d’une dissection ou d’un anévrysme de l’aorte thoracique, en l’absence d’éléments syndromique évocateurs. Elle doit également être complétée par un bilan morphologique des apparentés.
Introduction
La société européenne de cardiologie actualise, après 7 et 10 ans, ses recommandations sur la prise en charge de la maladie vasculaire périphériques et des pathologies aortiques.
Souvent asymptomatiques et sous diagnostiquées, les maladies vasculaires périphériques et aortiques sont des pathologies fréquentes. Ces pathologies représentent un marqueur de risque cardiovasculaire puissant associé à une augmentation de la mortalité toutes causes et à un risque accru d’événement cardiovasculaire majoré d’un facteur 4 à 5 par rapport aux sujets indemnes de maladie vasculaire périphérique. Les auteurs soulignent également l’importance de la nature systémique de la maladie vasculaire périphérique qui affecte l’ensemble de l’arbre vasculaire et l’importance des mesures non interventionnelles dans la stratégie thérapeutique.
L’évaluation des anévrismes aortiques requièrent une approche multiparamétrique. Leur prise en charge est guidée par le degré de dilatation de ce dernier confronté à de nombreux paramètres additionnels précisant le risque de complications aigues incluant la documentation d’une pathologie héritable.
1/ Maladie vasculaire périphérique
- I. Artériopathie oblitérante des membres inférieurs
Diagnostic et évaluation
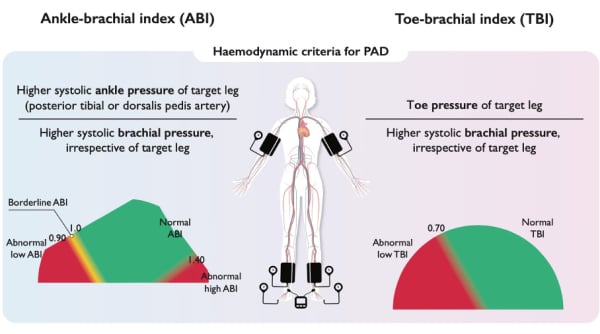
Le dépistage et le diagnostic de la maladie vasculaire périphérique repose sur la mesure de la pression artérielle aux 4 membres et le calcul de l’index cheville-biceps (figure 1). Cette mesure doit être réalisée en position allongée après 5 à 10 minutes de repos. Un rapport ≤0.90 confirme le diagnostic (grade IB). Secondairement, la réalisation d’une échographie Doppler confirme la localisation et la sévérité des lésions. En présence d’un index cheville-biceps> 1.40, ou en présence de facteurs de risque cardiovasculaire multiple, ce dépistage peut être complété par la mesure de l’index orteil-biceps ou la réalisation d’une imagerie Doppler d’emblée.
Figure 1 : diagnostic et évaluation de la maladie vasculaire périphérique
Prise en charge
Le traitement de l’artériopathie oblitérante des membres inférieurs symptomatique repose en 1ère intention sur l’intervention médicale (grade IB). Cette intervention est dominée par l’intensification de la surveillance et du contrôle des facteurs de risque cardiovasculaires : le contrôle de la pression artérielle <130/85 mmHg voire <120/80 mmHg, l’objectif d’HbA1c < 7.0%, une alimentation saine, la lutte contre le surpoids et l’obésité abdominale, ou encore la limitation de la consommation tabagique. De même, la prescription d’activité physique renforcée, et le recours aux thérapeutiques hypolipémiantes et anti-thrombotiques sont recommandées. La réalisation d’un geste de revascularisation est recommandée en 2nde ligne (grade IC). L’indication opératoire est guidée par la persistance des symptômes et l’impact sur la qualité de vie.
Le choix des modalités de revascularisation, chirurgicales ou interventionnelles, dépend de la nature et de la localisation des lésions. Les présentations d’ischémie aiguë et d’ischémie chronique menaçante (PA cheville <50 mmHg ; PA orteil <30 mmHg ; TcPO2 <30 mmHg) requièrent un diagnostic et une évaluation rapide pour la réalisation d’un geste de revascularisation urgent.
Chez les patients symptomatiques, la stratégie anti-thrombotique par simple anti-agrégation plaquettaire par aspirine faible dose (75 -160) mg ou par clopidogrel 75 mg, est privilégiée (grade IA). Dans cette indication, la supériorité du clopidogrel 75 mg est proposée (grade IIb). En alternative, l’association rivaroxaban 2.5 mg en 2 prises par jour et aspirine 100 mg est proposée chez les patients non à haut risque hémorragique (grade IIa). Cette dernière est également privilégiée au décours d’un geste de revascularisation (grade IIa) en alternative à une double anti-agrégation plaquettaire d’1 mois (grade IIb). En l’absence de contre-indication, chez des patients asymptomatiques en prévention primaire, une simple anti-agrégation plaquettaire par aspirine faible dose (75-100 mg) est proposée (grade IIb). Enfin, le recours à une double anti-agrégation plaquettaire au long cours n’est pas recommandée (grade III).
Les objectifs lipidiques sont abaissés à 0.55 g/L de LDL cholestérol avec un objectif de diminution de > 50% des valeurs basales (grade IA). Le recours à l’association statines/ezetimibe et l’ajout d’un inhibiteur des PCKS9 en cas d’objectif non atteint est recommandé (grade I). Le recours aux fibrates n’est pas recommandé (grade III).
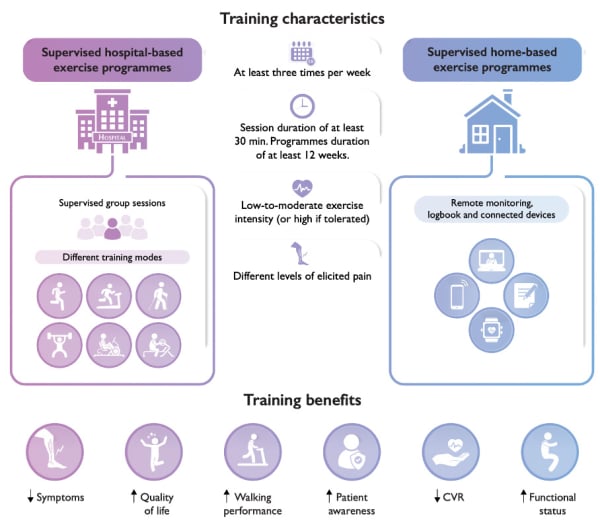
Le recours à l’activité physique est recommandé sous la forme de programmes stéréotypés de 3 séances hebdomadaires d’au moins 30 minutes d’effort pendant 12 semaines avec une augmentation progressive de l’intensité des séances guidée par le seuil de survenue des symptômes (figure 2).
Les auteurs insistent également sur la dimension familiale de cette pathologie avec des interventions non-médicamenteuses qui doivent être renforcées à l’ensemble du foyer pour une adhérence optimale.
Figure 2 : caractéristiques des programmes de réentrainement à l’effort dans la maladie vasculaires périphérique.
- II. Sténose carotidienne :
L’évaluation Doppler de la sténose carotidienne repose sur l’évaluation NASCET (grade I). La méthode ECST n’est plus recommandée (grade III).
Chez des patients présentant une sténose carotidienne symptomatique, la réalisation d’un geste de revascularisation est recommandée en cas de sténose évaluée entre 50 et 99% (grade IA pour les lésions entre 70-99 % et grade IIa pour les lésions évaluées entre 50-69%). L’intervention n’est pas recommandée en cas de lésion < 50% (grade III).
Chez des patients asymptomatiques, la réalisation d’un geste de revascularisation systématique n’est pas recommandée mais réservée aux patients à faible risque opératoire présentant une sténose évaluée entre 60 et 99% pour lesquels des facteurs de risque d’accident vasculaire cérébral (AVC) ont été identifiés (grade IIb). Les facteurs de risque d’AVC mentionnés sont dominés par : la présence d’un AVC silencieux homolatéral à l’imagerie cérébrale, les antécédents d’AIT/AVC controlatéral, la présence de plaques hypoéchogènes au Doppler ou encore l’identification d’hémorragie intraplaque à l’IRM (figure 4).
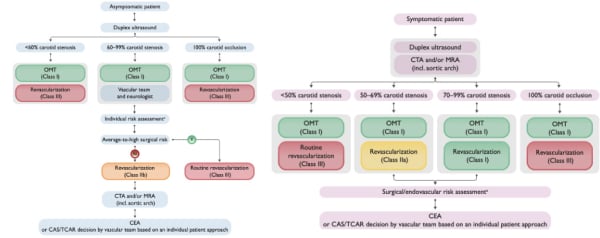
Figure 3 : sténose carotidienne, indications opératoires (à gauche patient asymptomatique, à droite patient symptomatique).
Figure 4 : Facteurs de risque d’accident vasculaire cérébral en présence d’une sténose carotidienne asymptomatique ³60%.
Le choix des modalités de revascularisation (endartériectomie ou stenting) repose sur une évaluation du risque opératoire et de la faisabilité d’un geste d’angioplastie par une évaluation multidisciplinaire.
Une double anti-agrégation plaquettaire par aspirine faible dose et clopidogrel (75 mg) est recommandée pour un délai minimal de 21 jours dans l’attente d’un geste de revascularisation carotidienne si le risque hémorragique le permet (grade IA). Cette bithérapie est à poursuivre pour une durée de 1 mois en cas de revascularisation par angioplastie (grade IA).
Au long cours, la prescription d’une simple anti-agrégation plaquettaire est recommandée chez les patients ayant bénéficié d’un geste et de revascularisation. Cette recommandation s’étend, en prévention primaire, en cas de sténose carotidienne asymptomatique > 50% si le risque hémorragique le permet (grade IIa).
Les objectifs de contrôle lipidique (diminution de > 50 % de LDLc et LDLc < 0.55 g/L) avec le recours aux stratégies médicamenteuses habituelles (statines, statines/ezetimibe, inhibiteur du PCSK9) sont renouvelés.
- III. Sténose des artères rénales :
La revascularisation des sténoses athéromateuses des artères rénales est maintenant recommandée en cas de sténose >70% en présence de facteurs de risque et après évaluation invasive confirmant la sévérité de la lésion (sténose >70% ou 50-69% avec retentissement hémodynamique). Les facteurs de risque mentionnés sont : la présence d’une lésion évolutive, d’une HTA résistante, d’un déclin rapide de la fonction rénale, d’un OAP flash ou la présence d’une sténose sur rein unique (grade IIa).
L’évaluation multiparamétrique de la viabilité rénale (taille, différenciation cortico médullaire, protéinurie, index de résistance) en vue d’un geste de revascularisation est également recommandée. En l’absence de critère de viabilité, la réalisation d’un geste de revascularisation n’est pas recommandée (grade III).
- IV. Sténose sous clavière :
L’artériopathie sous clavière est une pathologie fréquente et doit être suspectée en présence d’une asymétrie tensionnelle >10/15 mmHg. L’évaluation Doppler est la méthode d’évaluation de référence. Malgré l’absence de données issues de travaux randomisées, les stratégies interventionnelles sont privilégiées aux alternatives chirurgicales en raison d’un plus faible taux de complication à résultats équivalent (grade IIb).
2/ Pathologies aortiques
- I. Anévrysme de l’aorte thoracique ascendante
Évaluation
Bien que la meilleure méthode de mesure des diamètres aortiques soit encore débattue, la stratégie de référence reste la mesure du diamètre aortique télédiastolique bord interne à bord interne. La mesure bord externe à bord externe est néanmoins privilégiée en cas d’épaississement pathologique du mur aortique (athérome, thrombus, hématome, aortite). Dans l’évaluation de la racine aortique par imagerie de coupe (TDM, IRM), la mesure de fond de sinus à fond de sinus est la mieux corrélée avec les mesures échographiques mais d’autres alternatives sont possibles (fond de sinus à commissure). Un écart de diamètre >5 mm indique la présence d’une asymétrie de la racine, fréquent dans le cas des anévrysmes héritables et des anévrysmes sur valve bicuspide qu’il convient de rechercher.
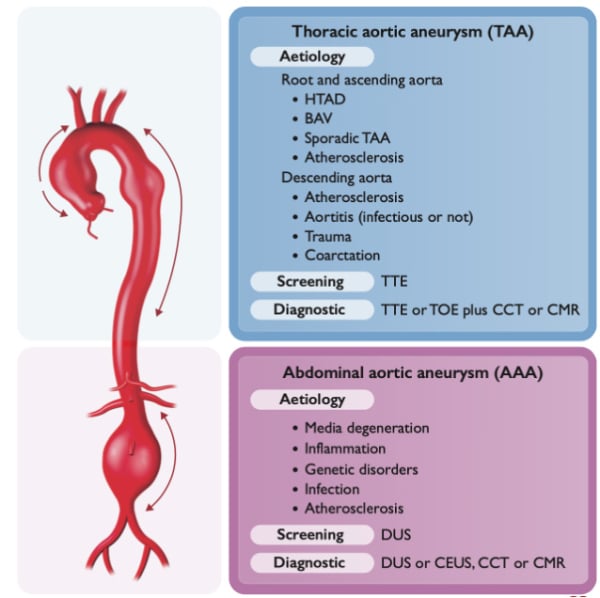
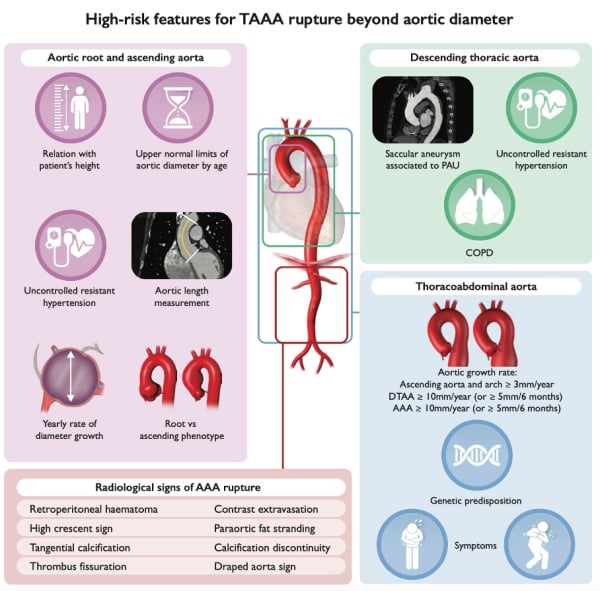
Figure 5 : anévrysme de l’aorte thoraco abdominale, étiologies, dépistage et diagnostic
Figure 6 : facteurs de risque de rupture d’anévrysme de l’aorte thoraco abdominale.
Indication opératoire :
Le seuil d’intervention chirurgical des anévrysmes de l’aorte ascendante, indifféremment de la morphologie valvulaire aortique tricuspide ou bicuspide, est abaissé à >52 mm chez des patients à faible risque opératoire (grade IIa). Le seuil de ³55 mm chez les patients tout venant est maintenu avec un niveau de preuve renforcé par rapport aux précédentes recommandations (grade I). Chez des patients à faible risque opératoire, ce seuil peut être diminué à ³50 mm en présence de facteurs de risque additionnel (grade IIb en cas de valve aortique tricuspide et IIa en cas de morphologie bicuspide) :
- Phénotype racine
- Âge < 50 ans
- Croissance ³ 3 mm/an
- Faible gabarit (< 1.69 m)
- Longueur de l’aorte ascendante > 11 cm
- HTA résistante
- Coarctation aortique (en cas de valve bicuspide)
- Antécédents familiaux d’évènement aortique aigu (en cas de valve bicuspide)
- Désir de grossesse
Enfin, le seuil d’intervention de ³45 mm est proposé en cas de coréalisation d’une chirurgie valvulaire aortique, majoré à ³50 mm pour des patients bénéficiant d’une chirurgie cardiaque non valvulaire aortique (grade IIa).
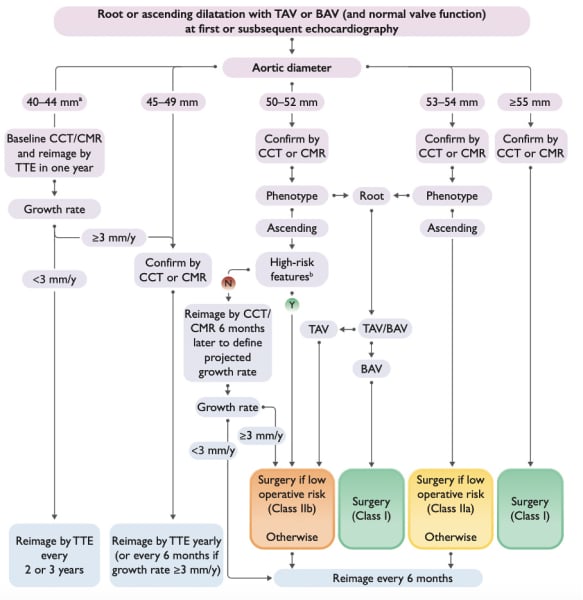
Figure 7 : anévrysme de l’aorte ascendante non héritable, algorithme de prise en charge (TAV : valve aortique tricuspide ; BAV : valve aortique bicuspide). b Pour les valves tricuspide comme bicuspide : âge < 50 ans, taille < 1.69 m, hauteur aortique >11cm, HTA non contrôlée et en cas de valve bicuspide : coarctation aortique et histoire familiale d’évènement aortique aigu.
Populations particulières :
- Syndrome de Marfan : l’indication chirurgicale est recommandée en cas de diamètre aortique maximal mesuré au niveau des valsalvas ³ 50 mm (grade IB). Ce seuil est abaissé à 45 mm en présence des facteurs suivants : antécédent familial de dissection aortique pour des faibles diamètres, hypertension nécessitant ³3 traitements, progression ³3 mm/an et/ou de désir de grossesse. Le seuil d’intervention de ³50 mm est proposé en cas de dilatation anévrysmale de l’aorte thoraco abdominale (grade IIa).
- Syndrome d’Ehlers-Danlos vasculaire : les décisions de suivi et d’intervention thérapeutique relèvent d’une discussion d’expert. Les données disponibles à ce jour ne permettent pas de soutenir des seuils d’intervention précis pouvant justifier d’une chirurgie aortique prophylactique en présence d’une dilatation anévrysmale. La prescription de Celiprolol prévient les évènements vasculaires et est proposée (grade IIa).
- Syndrome de Turner : la décision d’intervention est guidée par des mesures indexées aux gabarits des patientes avec une intervention recommandé en cas de dilatation aortique >23 mm/m2, >23 mm/m, et de z-score >3.5 en présence de facteur de risque de dissection et/ou de désir de grossesse ou, en l’absence de facteurs additionnels, de dilatation aortique >25 mm/m2, >25 mm/m, z-score >4.0
- Syndrome Loeys-Dietz / mutation TGFb : l’intervention est recommandée à partir du seuil de 45 mm (grade IIa) et peut-être proposée à partir du seuil de 42 mm en présence de facteurs spécifiques (variant à risque, histoire familiale, progression anévrysmale). Une surveillance échographique drastique tous les 6 à 12 mois en recommandée.
- Mutations des gènes de l’alpha-actine (ACTA2) et SMC : l’intervention est recommandée à partir du seuil de 45 mm (grade IIa).
Traitement médical
La correction chirurgicale d’un anévrysme de l’aorte ascendante requiert une simple anti-agrégation plaquettaire par aspirine faible dose (75-100mg) dans les 3 premiers mois suivant l’intervention (grade IIa). Le suivi post opératoire nécessite la réalisation d’une imagerie TDM de référence <1 mois après l’intervention à répéter annuellement pendant les 2 premières années post intervention.
Le recours au traitement médical par bêta-bloquants ou par bloqueur du système rénine angiotensine est recommandé chez les patients présentant un syndrome de Marfan afin de prévenir la dilatation aortique (grade I) et l’association des 2 molécules est à considérer (grade IIa).
En revanche, en l’absence de pathologie aortique héritable identifiée, le traitement préventif d’un anévrysme de l’aorte ascendante rejoint les stratégies de prévention primaire recommandée : sevrage tabagique, activité physique et contrôle de la pression artérielle (< 140/90 mmHg voire <120/80 mmHg si toléré). En l’absence d’autre indication, le recours au traitement par statines faible dose est proposé pour diminuer le risque de complications liées à l’anévrysme. En revanche, le traitement par aspirine faible dose est débattu mais semble raisonnable chez des patients présentant d’autres comorbidités cardiovasculaires.
Chez les patientes présentant un syndrome de Marfan avec un désir de grossesse, les stratégies de conseil génétique, d’évaluation pré conceptionnelle et la poursuite d’un traitement par beta bloquant lors de la grossesse sont recommandées (grade I).
Dépistage, bilan génétique et surveillance :
Devant la découverte d’un anévrysme de l’aorte ascendante ou d’une dissection de l’aorte thoracique, une enquête familiale systématique sur au moins 3 générations est recommandée. La présence d’un antécédent d’anévrysme de l’aorte thoracique, d’une mort subite inexpliquée <60 ans, d’un anévrysme périphérique ou intracrânien doit faire motiver la réalisation d’un bilan génétique du cas index (grade I) et la réalisation d’un bilan morphologique, à minima par échographie transthoracique, chez les apparentés.
En présence d’un variant pathologique identifié chez le cas index, la réalisation d’un dépistage génétique chez les apparentés est recommandé. En l’absence de variant pathologique documenté chez le cas index, la réalisation d’une imagerie aortique est recommandée à partir de l’âge de 25 ans (ou 10 ans avant le cas familial index si ce dernier avait eu lieu à un âge précoce), à renouveler tous les 5 ans jusqu’à l’âge de 60 ans en cas de dépistage négatif (grade IIa).
En cas de dilatation >40 mm, la surveillance d’un anévrysme de l’aorte ascendante repose sur la réalisation d’une imagerie régulière annuelle (grade IIa). Il est recommandé d’établir le suivi évolutif d’un anévrysme par les mêmes modalités d’imagerie (IC). Le suivi échographique est possible dans le cas des anévrysmes de l’aorte thoracique ascendante et la confirmation par IRM ou imagerie scanner est recommandé en cas d’évolutivité. La surveillance d’un anévrysme de l’aorte thoracique descendante et de l’aorte abdominale nécessite la réalisation d’une imagerie IRM ou TDM.
En cas de dilatation >40 mm associé à une valve aortique de morphologie bicuspide, un contrôle à 1 an est recommandé et à renouveler tous les 2 à 3 ans en l’absence d’évolutivité.
- II. Anévrysme de l’aorte thoraco-abdominale
Anévrysme de l’aorte thoracique non ascendante
Ces recommandations font état des modalités d’évaluation et de prise en charge des anévrysmes de l’aorte thoraco-abdominale. En l’absence d’élément confirmant le diagnostic de syndrome aortique aigu, la décision opératoire est guidée par : la présence de douleurs thoraciques, la sévérité de la dilatation anévrysmale documentée par imagerie IRM/TDM (³ 55 mm pour l’arche et l’aorte thoracique descendante), la localisation et l’extension de la dilatation anévrysmale et le risque opératoire du patient.
Le choix des modalités de correction de l’anévrysme par réparation chirurgicale ouverte ou par remplacement endovasculaire type TEVAR (« Thoracic Endovascular Aortic Aneurysm repair ») dépend de plusieurs caractéristiques (localisation, extension de l’anévrysme, risque opératoire…). L’intervention chirurgicale ouverte revêt d’une morbi mortalité post opératoire importante, estimée entre 6 et 10%, et doit être réservée à des centres experts.
Anévrysme de l’aorte abdominale
De même, ces recommandations précisent les indications et les modalités de prise en charge des anévrysmes de l’aorte abdominale. Les seuils d’intervention de ³55 mm chez les hommes, ³50 mm chez les femmes et ³45 mm en cas d’anévrysme sacciforme sont proposés. La décision opératoire et le choix de la modalité d’intervention dépendent de la présentation anatomique de la lésion, du risque opératoire et des préférences du patient. La progression >5 mm / 6 mois est associée à un risque d’événement plus important et doit faire considérer l’intervention.
Le dépistage opportuniste de l’anévrysme de l’aorte abdominale est recommandé chez tout patient éligible à une politique de dépistage échographique de maladie vasculaire périphérique.
- III. Dissection aortique et syndrome aortique aigu
Diagnostic
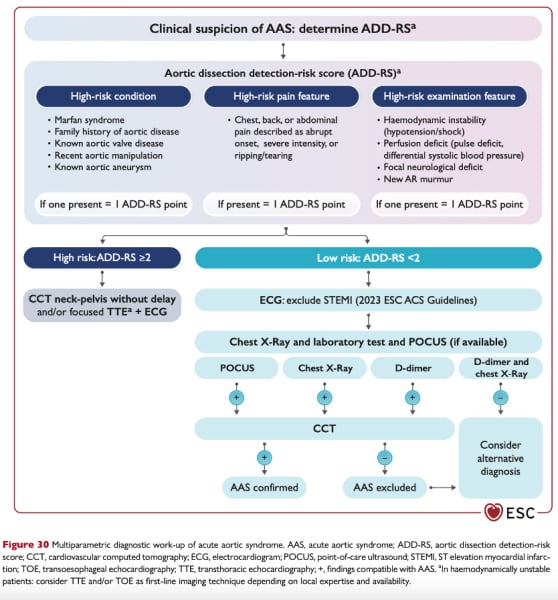
Le diagnostic précoce est un des enjeux essentiels de la prise en charge des patients présentant un syndrome aortique aigu (figure 8). Devant une présentation clinique compatible avec un syndrome aortique aigu, l’utilisation de l’algorithme ADD-RS (« acute dissection detection risk score ») pour confirmer ou non le diagnostic est recommandé (grade IB). Ces recommandations précisent que l’élévation des D-Dimères en deçà du seuil de 500 ng/mL rend le diagnostic de dissection aortique aigue peu probable.
Figure 8 : Algorithme ADD-RS « acute dissection detection risk score »
Prise en charge (figure 9)
En cas de dissection aortique de type A, le traitement chirurgical reste la stratégie de référence (grade IB). La réalisation d’une échographie transoesophagienne per opératoire est recommandée pour détecter la présence de complication, préciser la nature du geste à réaliser, préciser l’extension proximale de la dissection et ainsi guider l’indication d’un geste de remplacement ou de réparation valvulaire (grade I).
Chez des patients présentant une dissection aortique aigue de type B, l’intervention est recommandée dans un délai rapide en présence de complications et/ou de signe de mauvaise perfusion (grade IB). La réparation endovasculaire type TEVAR (« Thoracic Endovascular Aortic Aneurysm repair ») est la stratégie de référence chez les patients éligibles. En l’absence de complication, l’intervention est recommandée dans un délai de 14 à 90 jours, et l’indication guidée par la présence de facteurs de risque de complication aortique (grade IIa) : diamètre aortique >40 mm, diamètre total >50 mm, signe de mauvaise perfusion, faux chenal >20/22 mm ou la récidive de symptômes.
En l’absence d’indication opératoire ou chez des patients présentant une dissection chronique de type B (>3 mois après le début des symptômes), l’intervention est recommandée en cas d’évolution des symptômes, de progression anévrysmale ³60 mm (grade IB) ou ³55 mm chez des patients à faible risque opératoire (grade IIa). Les stratégies endovasculaires sont privilégiées.
De la même manière, en cas d’extension d’une dissection de la crosse aorte à sa portion descendante proximale, le recours aux prothèses type « elephant trunk » est recommandé (grade IIa).
Les autres présentations de syndrome aortique aigus (ulcère pénétrant, hématome intra mural) relèvent du même type de prise en charge. L’indication chirurgicale est guidée par l’évolution des symptômes, la présence de signe de mauvaise perfusion et par l’évolutivité des lésions aux contrôles d’imagerie.
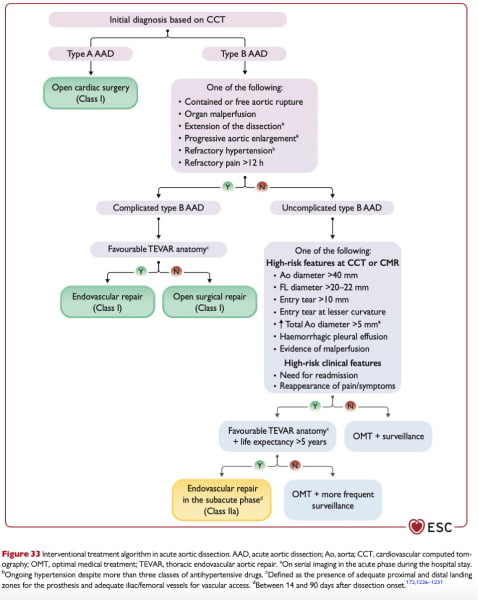
Figure 9 : Dissection aortique aigue, recommandations de prise en charge, ESC 2024.