17 minutes de lecture
Recommandations pour l’évaluation cardiovasculaire avant une chirurgie non-cardiaque
Publié le dimanche 28 août 2022
En direct de l'ESC Congress 2022
Chaque année dans le monde, environ 300 millions de patients (soit 5 % de la population mondiale) bénéficient d’une chirurgie. Dans 85 % des cas, cette chirurgie est non-cardiaque. Or, de précédentes études ont démontré qu’une majorité de patients de plus de 45 ans bénéficiant d’une chirurgie non-cardiaque ont au moins 2 facteurs de risque cardiovasculaire, 18 % ont une maladie coronaire, et près de 5 % ont un antécédent d’AVC1.
De plus, près de 1 % des chirurgies se compliquent d’un décès au cours de la période péri-opératoire, dont la moitié environ est d’origine cardiovasculaire. Les comorbidités du patient, sa capacité fonctionnelle, le degré d’urgence, le type de chirurgie et sa durée déterminent le risque de complications péri-opératoires.
Très attendues, ces nouvelles recommandations sur l’évaluation cardiovasculaire avant une chirurgie non-cardiaque viennent actualiser celles de 20142. Rédigées conjointement par la Société Européenne de Cardiologie (ESC) et la Société Européenne d’Anesthésiologie et de Réanimation (ESAIC)3, elles répondent à une situation fréquemment rencontrée en pratique clinique, dans le but de diminuer la morbimortalité péri-opératoire.
Les 10 points clés
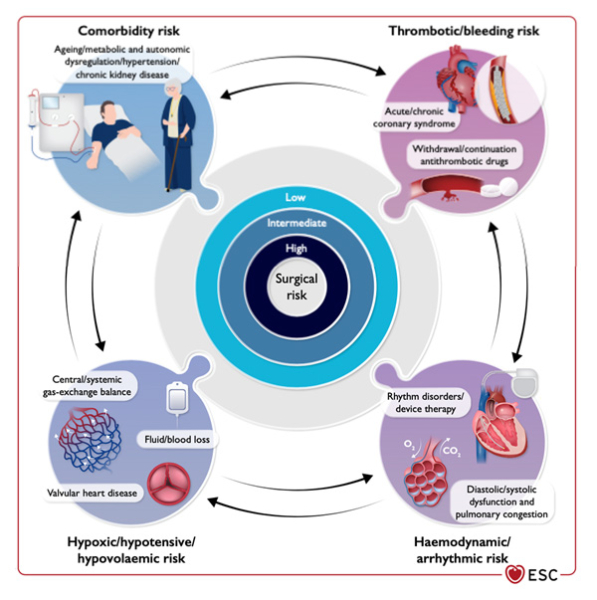
- La survenue de complications cardiovasculaires en péri-opératoire d’une chirurgie non-cardiaque n’est pas rare et exerce un impact considérable sur le pronostic. Il est donc primordial d’en évaluer le risque, en se basant sur l'analyse complète des facteurs de risque liés au patient, et des facteurs de risque liés à la chirurgie (type de chirurgie et degré d’urgence)
- L’identification et la gestion des facteurs de risque liés au patient permettent de réduire le risque péri-opératoire
- La prise en compte des facteurs liés à la chirurgie permet de classer les chirurgies à risques faible, intermédiaire et élevé
- L’examen clinique, l’évaluation de la capacité fonctionnelle, et le recours à certains tests non-invasifs (ECG, ETT, biomarqueurs cardiaques) représentent la pierre angulaire de l’évaluation du risque pré-opératoire
- Ces nouvelles recommandations se positionnent en faveur du dosage de la troponine chez tout patient avec une maladie cardiovasculaire, ou en présence d’un facteur de risque cardiovasculaire (dont un âge ≥ 65 ans) avant une chirurgie à risque intermédiaire ou élevé, et 24 à 48 heures après l’intervention, dans le but de détecter précocement un infarctus du myocarde péri-opératoire
- Le traitement des maladies cardiovasculaires et des facteurs de risque cardiovasculaires doit être individualisé en fonction du risque pré-opératoire et effectué en fonction des recommandations en vigueur
- Une évaluation multidisciplinaire du timing de la chirurgie chez des patients à haut risque bénéficiant d’une chirurgie à haut risque est recommandée
- Chez les patients sous traitement anti-thrombotique, l’évaluation précise et individualisée de la balance entre le risque ischémique et le risque hémorragique est primordiale, afin de l’adapter avant la chirurgie
- La gestion du traitement médicamenteux avant une chirurgie non-cardiaque vise à éviter un déséquilibre hémodynamique et une perturbation d’une pathologie cardiovasculaire chronique lors de la période péri-opératoire
- L’identification d’une complication cardiovasculaire péri-opératoire, en particulier d'une souffrance myocardique péri-opératoire, doit déclencher un algorithme de prise en charge diagnostique et thérapeutique spécifique permettant d’en identifier la cause et de la traiter
Figure 1 - Prise en compte des facteurs liés à la chirurgie permettant de classer les chirurgies à risques faible, intermédiaire et élevé
1. Évaluation pré-opératoire
Évaluation clinique
L’évaluation du risque de morbimortalité pré-opératoire en chirurgie non-cardiaque inclut l’évaluation des risques liés au patient, et des risques liés à la chirurgie.
Les risques liés à la chirurgie sont déterminés par le type et la durée de la chirurgie, son degré d’urgence (urgence immédiate, urgence, semi-urgence et programmée), et le type d’anesthésie.
Toute chirurgie s’accompagne d’une augmentation des taux de cortisol et de catécholamines en réponse au stress induit par les lésions tissulaires et l’inflammation, ainsi que d’un déséquilibre des balances sympathovagale et neuroendocrine. Les modifications de la température corporelle, la perte sanguine et l’hypovolémie peuvent diminuer les résistances vasculaires et induire une hypotension, menant à un déséquilibre entre les besoins et les apports en oxygène au myocarde. Les saignements, la transfusion, les lésions tissulaires et l’inflammation, qui peuvent survenir au cours d’une chirurgie, peuvent activer les processus de coagulation, et ainsi entrainer un état prothrombotique.
Ainsi, les procédures vidéo-assistées, comme les thoracoscopies en chirurgie thoracique, et les procédures endovasculaires en chirurgie vasculaire, qui permettent de réduire le degré de lésion tissulaire, doivent être privilégiées chez les patients à haut risque cardiovasculaire (grade IIa).
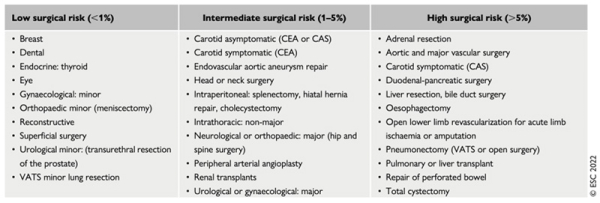
Selon le type de chirurgie, on individualise celles à risques faible, intermédiaire et élevé :
Figure 2 - Tableau présentant les caractéristiques des chirurgies à risques faible, intermédiaire et élevé
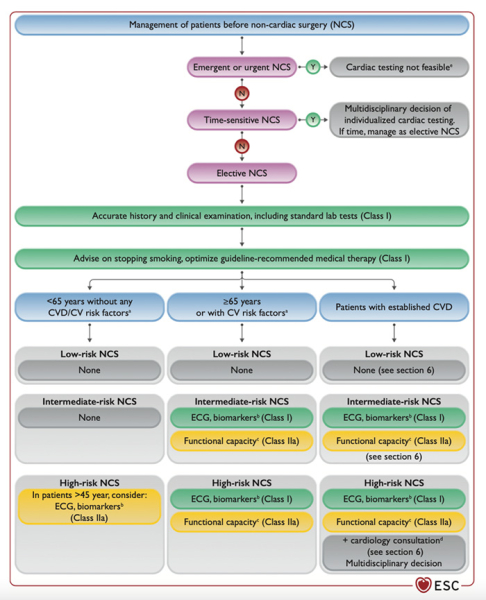
Les risques liés au patient sont déterminés par l’âge, la présence ou non de facteurs de risque cardiovasculaires ou de maladies cardiovasculaires établies, et les autres comorbidités. Tout patient bénéficiant d’une chirurgie non-cardiaque doit bénéficier d’une évaluation précise et d’un examen clinique exhaustif, associés à une évaluation du risque pré-opératoire (grade I). Si le temps le permet, il est recommandé d’optimiser le traitement des maladies cardiovasculaires et des facteurs de risque cardiovasculaires avant la chirurgie (grade I). L’attitude doit ensuite s’adapter à la situation :
- Chez les patients de moins de 65 ans sans signe, symptôme ou antécédent de maladie cardiovasculaire : un ECG et la mesure des biomarqueurs cardiaques doivent être discutés uniquement après 45 ans, et en cas de chirurgie à risque élevé (grade IIa). En cas d’histoire familiale de cardiomyopathie d’origine génétique, il est recommandé de réaliser un ECG et une ETT avant la chirurgie, quel que soit l’âge ;
- Chez les patients de 65 ans et plus, ou ceux avec maladie cardiovasculaire établie, l’évaluation pré-opératoire dépend du niveau de risque de la chirurgie ;
- En cas de découverte d’un souffle cardiaque au cours de l’évaluation pré-opératoire, il est recommandé de réaliser une ETT avant la chirurgie si d’autres symptômes ou signes de maladie cardiovasculaire sont présents (grade I) ;
- En cas de découverte d’un angor avant une chirurgie programmée, il est recommandé d’avoir recours à l’algorithme diagnostique de la maladie coronaire chronique (grade I). Si la chirurgie est urgente, une évaluation multidisciplinaire est recommandée (grade I) ;
- En cas de découverte d’une dyspnée ou d’un œdème périphérique, un ECG et un dosage du NT-proBNP/BNP sont recommandés (grade I). En cas d’élévation du NT-proBNP/BNP, une ETT est recommandée (grade I).
Dans tous les cas, il est recommandé de délivrer une information individualisée au patient concernant les modifications de ses traitements en péri-opératoire, sous formes verbale et écrite (grade I), en utilisant des outils de type check-list, en particulier chez les patients à haut risque de complications cardiovasculaires (grade IIa).
Figure 3 - Gestion des patients avant une chirurgie non-cardiaque
Outils de l’évaluation pré-opératoire
Les scores de risque
Plusieurs indices de risque ont été développés pour intégrer les facteurs de risque liés au patient, et ceux liés à la chirurgie. Ces nouvelles recommandations ne se positionnent pas pour l’utilisation spécifique d’un score de risque. En revanche, l’évaluation de la fragilité par des outils de screening validés doit être envisagée chez les patients de plus de 70 ans (grade IIa).
L’ECG et les biomarqueurs cardiaques
Chez les patients d’un âge supérieur ou égal à 65 ans, ou en présence d’une maladie cardiovasculaire, d’au moins un facteur de risque cardiovasculaire, ou de symptômes ou signes de maladie cardiovasculaire, il est recommandé de réaliser un ECG 12 dérivations avant une chirurgie de risque intermédiaire ou élevé (grade I).
Chez les patients d’un âge supérieur ou égal à 65 ans, ou en présence d’une maladie cardiovasculaire, d’au moins un facteur de risque cardiovasculaire, ou de symptômes ou signes de maladie cardiovasculaire, il est recommandé de doser la troponine avant une chirurgie de risque intermédiaire ou élevé (grade I). Dans cette situation, le dosage du NT-proBNP/BNP doit être également envisagé (grade IIa).
Chez les patients à bas risque bénéficiant d’une chirurgie à risque faible ou intermédiaire, il n’est pas recommandé d’effectuer un ECG, ni un dosage de troponine ou NT-proBNP/BNP (grade III).
Examens cardiaques non invasifs
Une ETT est recommandée chez les patients avec une capacité fonctionnelle abaissée et/ou une élévation du NT-proBNP/BNP, ou si un souffle cardiaque de novo a été détecté avant une chirurgie à haut risque (grade I).
Une ETT doit également être envisagée en cas de maladie cardiovasculaire suspectée, ou de signes ou symptômes avant une chirurgie à haut risque (grade IIa). Avant une chirurgie à risque intermédiaire, une ETT peut être envisagée uniquement en cas de capacité fonctionnelle abaissée, d’ECG anormal, d’élévation du NT-proBNP/BNP, ou en présence d’au moins un facteur de risque clinique (grade IIb). En dehors de ces situations, une ETT à titre systématique n’est pas recommandée avant une chirurgie non-cardiaque (grade III).
Une imagerie de stress (échographie de stress, scintigraphie myocardique, IRM de stress) est recommandée avant une chirurgie à haut risque en cas de capacité fonctionnelle abaissée et de forte probabilité de maladie coronaire (grade I). Une imagerie de stress doit être envisagée avant une chirurgie à haut risque chez des patients asymptomatiques avec capacité fonctionnelle abaissée ou antécédent d’angioplastie coronaire ou de pontage aortocoronaire (grade IIa). Une imagerie de stress peut être discutée avant une chirurgie à risque intermédiaire en cas de suspicion d’ischémie myocardique chez des patients avec des facteurs de risque ou une capacité fonctionnelle abaissée (grade IIb). Dans toutes les autres situations, le recours à une imagerie de stress n’est pas recommandé (grade III). L’épreuve d’effort simple sur tapis ou cycloergomètre n’est pas recommandée dans l’évaluation pré-opératoire.
Le coroscanner peut être envisagé pour éliminer une maladie coronaire en cas de probabilité clinique faible ou intermédiaire chez les patients ne pouvant pas bénéficier d’une imagerie fonctionnelle avant une chirurgie non urgente à risque intermédiaire ou élevé (grade IIa).
Examens cardiaques invasifs
Il est recommandé de suivre les mêmes indications de coronarographie et de revascularisation myocardique avant une chirurgie que dans un contexte non-opératoire (grade I).
Une coronarographie pré-opératoire peut être discutée chez les patients avec une maladie coronaire chronique stable bénéficiant d’une endartériectomie carotidienne programmée (grade IIb).
Une coronarographie pré-opératoire n’est pas recommandée en cas de maladie coronaire chronique stable chez un patient bénéficiant d’une chirurgie à risque faible ou intermédiaire (grade III).
2. Stratégies de réduction du risque péri-opératoire
Gestion des facteurs de risque cardiovasculaire
Un arrêt du tabagisme au moins 4 semaines avant une chirurgie non-cardiaque est recommandé, dans le but de réduire le risque de mortalité et de complications péri-opératoires (grade I). Le contrôle des autres facteurs de risque (HTA, dyslipidémie, diabète) est également recommandé (grade I).
Gestion du traitement médicamenteux (hors anti-thrombotiques)
Introduction de statines ou bétabloquants
En cas d’indication d’un traitement hypolipémiant, l’introduction d’une statine doit être envisagée (grade IIa).
L’introduction d’un traitement bétabloquant avant une chirurgie à haut risque peut être discutée pour réduire le risque d’infarctus du myocarde péri-opératoire chez les patients ayant au moins 2 des facteurs suivants : maladie coronaire, maladie neurovasculaire, insuffisance rénale, diabète (grade IIb). En dehors de ces situations, l’introduction d’un bétabloquant n’est pas recommandée (grade III).
Les traitements à poursuivre
Il est recommandé de poursuivre les bétabloquants et les statines lors d’une chirurgie non-cardiaque (grade I).
Chez les patients avec une insuffisance cardiaque stable, la poursuite des médicaments agissant sur le système rénine-angiotensine peut être envisagée (grade IIb).
Les traitements à arrêter
Chez les patients sans insuffisance cardiaque, l’arrêt des médicaments agissant sur le système rénine-angiotensine et des diurétiques doit être envisagé le jour de la chirurgie, pour diminuer le risque d’hypotension péri-opératoire (grade IIa). Il doit être envisagé d’arrêter les inhibiteurs de SGLT2 au moins 3 jours avant une chirurgie à risque intermédiaire ou élevé (grade IIa).
Gestion des traitements anti-thrombotiques
La gestion du traitement antithrombotique doit se faire à la lumière de l’évaluation du risque thrombotique et du risque hémorragique.
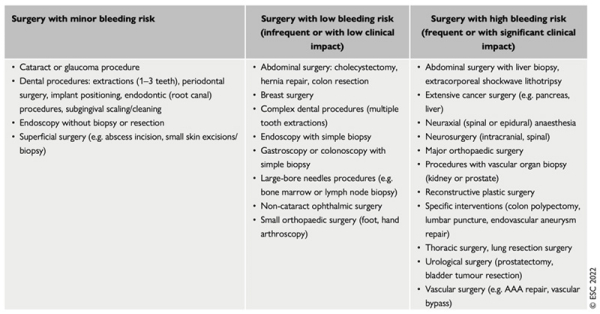
Le risque hémorragique dépend du type de chirurgie :
Figure 4 - Classification du risque hémorragique en cas de chirurgie
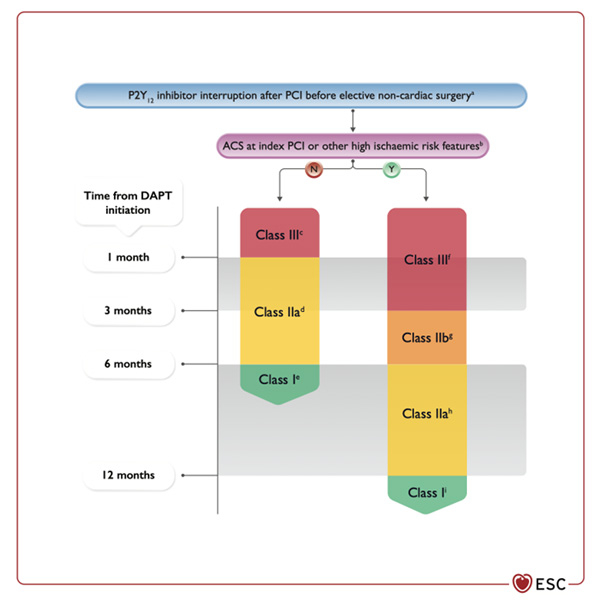
Le risque thrombotique dépend du délai depuis la dernière angioplastie coronaire, et du contexte de celle-ci (syndrome coronaire aigu vs maladie coronaire chronique) :
Figure 5 - Évaluation du risque thrombotique d'après le contexte de la dernière angioplastie coronaire
Gestion des anti-agrégants plaquettaires
Il est recommandé de décaler une chirurgie non-urgente au moins 1 mois, et au mieux 6 mois, après une angioplastie coronaire programmée, et au moins 3 mois, et au mieux 12 mois après un syndrome coronaire aigu (grade I).
Chez les patients ayant un antécédent d’angioplastie coronaire, il est recommandé de poursuivre le traitement par aspirine si le risque hémorragique le permet (grade I).
Si un arrêt d’inhibiteur de P2Y12 est nécessaire, il est recommandé un délai d’arrêt avant la chirurgie selon la molécule (grade I) :
- 3 à 5 jours pour le ticagrelor ;
- 5 jours pour le clopidogrel ;
- 7 jours pour le prasugrel.
Si un arrêt de l’aspirine est nécessaire avant une chirurgie à haut risque hémorragique (chirurgie intracrânienne, médullaire, intra-vitréenne ou rétinienne), il est recommandé d’arrêter l’aspirine au moins 7 jours avant la chirurgie (grade I).
Chez les patients sans antécédent d’angioplastie coronaire, il peut être discuté d’arrêter l’aspirine 3 jours avant la chirurgie, si le risque hémorragique surpasse le risque thrombotique (grade IIb).
Si le traitement anti-agrégant plaquettaire a été arrêté avant la chirurgie, il est recommandé de le reprendre dès que possible, dans les 48 heures suivant la chirurgie, et en accord avec l’évaluation multidisciplinaire du risque hémorragique (grade I).
Gestion des anticoagulants
Si une chirurgie urgente est nécessaire, il est recommandé d’arrêter sans délai les anticoagulants oraux directs (AOD) (grade I). L’idarucizumab (antidote du dabigatran) doit être discuté chez les patients sous dabigatran nécessitant une chirurgie urgente à risque hémorragique intermédiaire ou élevé (grade IIa).
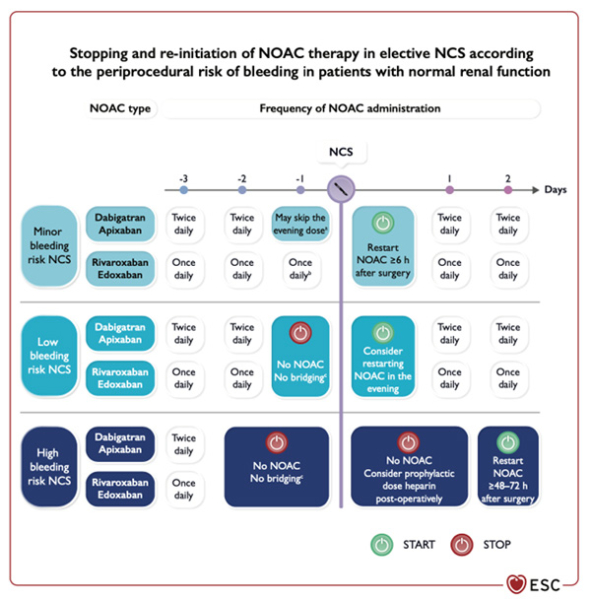
En cas de chirurgie à risque hémorragique non négligeable, il est recommandé d’arrêter les AOD selon la molécule, la fonction rénale et le risque hémorragique (cf. Figure 6) (grade I).
En cas de chirurgie à très haut risque hémorragique, l’arrêt des AOD au moins 5 demi-vies avant la chirurgie, et leur reprise au moins 24 heures après l’intervention, doivent être envisagés (grade IIa).
En cas de chirurgie à risque hémorragique mineure, il est recommandé de poursuivre les anticoagulants (grade I). En présence d’une valve mécanique, un relais doit être envisagé si l’arrêt de l’anticoagulant oral est nécessaire chez les patients avec une valve mécanique aortique si un facteur de risque thrombotique est présent, ou que la prothèse mécanique est d’ancienne génération, ou en cas de valve mécanique en position mitrale ou tricuspide (grade IIa).
Pour le relais, les HBPM sont recommandées en alternative aux HNF (grade I). Un relais de l’anticoagulation orale n’est pas recommandé chez les patients avec un risque thrombotique faible ou modéré (grade III).
Si le risque hémorragique post-opératoire est supérieur au risque thrombotique, il peut être discuté un arrêt de l’anticoagulant dans les 48 à 72 heures après l’intervention (grade IIb). L’utilisation d’une dose réduite d’AOD, si celle-ci n’est pas indiquée dans le but de réduire le risque hémorragique, n’est pas recommandée (grade III).
Figure 6 - Arrêt et ré-initiation du traitement par AOD lors d'une chirurgie non-cardiaque élective en fonction du risque péri-procédural d'hémorragie chez les patients à fonction rénale normale
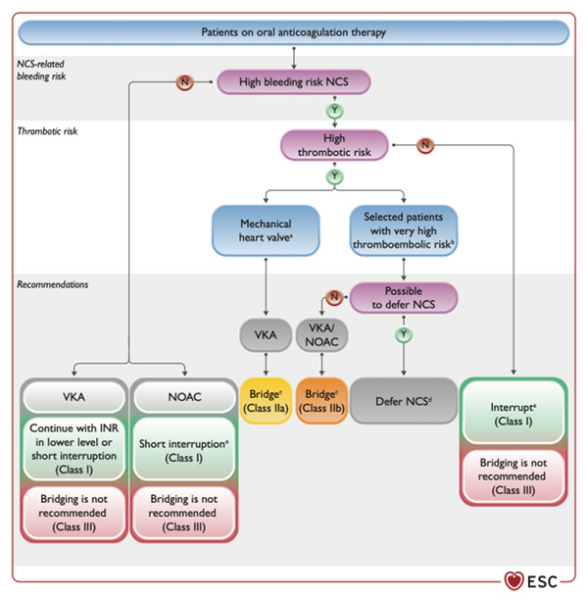
Figure 7 - Gestion des patients les patients sous traitement anticoagulant oral
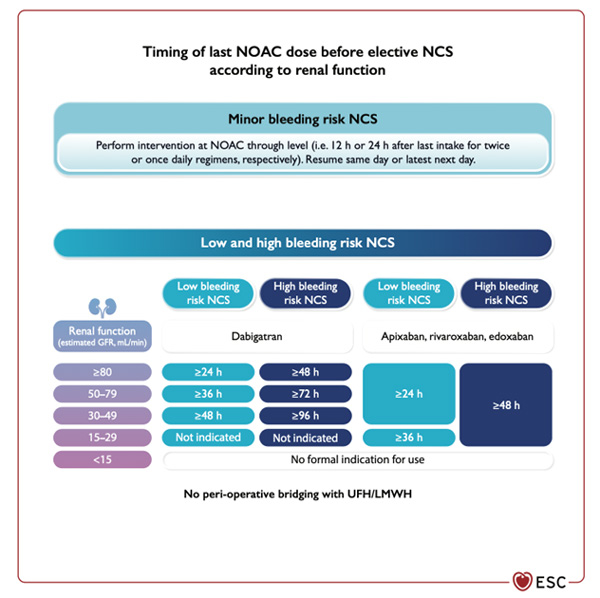
Figure 8 - Prise de la dernière dose d'AOD avant une chirurgie non-cardiaque élective d'après la fonction rénale
Thromboprophylaxie péri-opératoire
Si une thromboprophylaxie péri-opératoire est jugée nécessaire, il est recommandé de l’adapter selon le type de chirurgie, la durée d’immobilisation et les facteurs de risque du patient (grade I). Pour les patients à risque hémorragique faible, une thromboprophylaxie de 14 et 35 jours doit être envisagée en cas de chirurgie du genou et de la hanche, respectivement (grade IIa). Des AOD à dose réduite peuvent être envisagés en alternative aux HBPM pour la thromboprophylaxie post-opératoire de chirurgie de genou ou de hanche (grade IIb).
Gestion de l’anémie et des pertes sanguines péri-opératoires
Il est recommandé de mesurer l’hémoglobine en pré-opératoire d’une chirurgie à risque intermédiaire ou élevé (grade I). En cas d’anémie, il est recommandé de la traiter avant la chirurgie (grade I).
En cas de chirurgie avec perte sanguine attendue d’au moins 500 ml, l’utilisation d’un dispositif d’autotransfusion per-opératoire (cell-saver) est recommandée (grade I). En cas de chirurgie avec saignement majeur, l’administration d’acide tranexamique doit être envisagé (grade IIa). Une hémostase méticuleuse devrait être effectuée systématiquement (grade IIa).
Principales situations spécifiques
Maladie coronaire
Chez les patients avec maladie coronaire chronique, si une angioplastie coronaire est indiquée avant une chirurgie non-cardiaque, celle-ci doit être faite avec des stents actifs de nouvelle génération (grade I). Une revascularisation myocardique avant une chirurgie à haut risque peut être discutée selon la masse myocardique à risque, l’existence de symptômes, et l’anatomie coronaire à la coronarographie (grade IIb). Une revascularisation myocardique n’est pas recommandée en routine avant une chirurgie à risque faible ou intermédiaire (grade III).
Chez les patients avec syndrome coronaire aigu, il est recommandé de décaler, si possible, la chirurgie d’au moins 3 mois (grade I). Dans les rares cas où un syndrome coronaire aigu sans sus-décalage du segment ST survient simultanément à une situation nécessitant une chirurgie non-cardiaque urgente, la priorité pour la chirurgie doit être discutée au cas par cas, de manière multidisciplinaire (grade IIa).
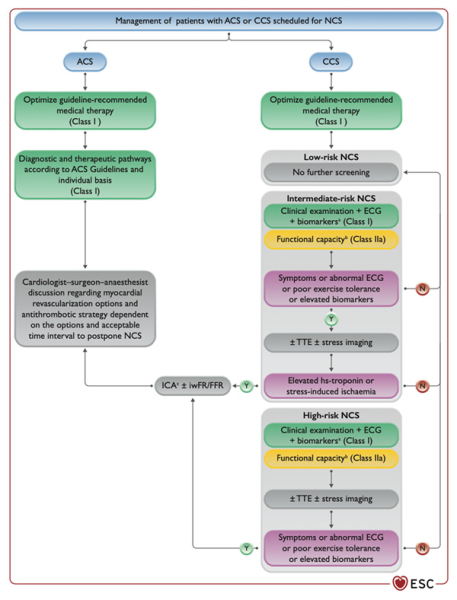
Figure 9 - Prise en charge des patients souffrant d'un syndrome coronaire aigu (SCA) et d'un syndrome coronarien chronique (SCC) devant subir une chirurgie non-cardiaque
Insuffisance cardiaque
Chez les patients avec insuffisance cardiaque suspectée ou connue bénéficiant d’une chirurgie à haut risque, il est recommandé d’évaluer la fonction ventriculaire gauche par une ETT et de doser le NT-proBNP/BNP (grade I). Ces patients doivent bénéficier du traitement de fond de l’insuffisance cardiaque, en accord avec les recommandations spécifiques (grade I), et d’une évaluation régulière en péri-opératoire du statut volémique et des signes de perfusion périphérique (grade I).
Chez les patients avec assistance cardiocirculatoire, une évaluation multidisciplinaire est nécessaire (grade I).
Valvulopathies
Chez les patients avec rétrécissement aortique sévère symptomatique en attente de chirurgie programmée à risque intermédiaire ou élevé, un remplacement valvulaire aortique chirurgical ou percutané (TAVI) est recommandé avant la chirurgie (grade I).
Chez les patients avec rétrécissement aortique sévère asymptomatique en attente de chirurgie programmée à risque élevée, un remplacement valvulaire aortique chirurgical ou percutané (TAVI) doit être envisagé avant la chirurgie (grade IIa).
Chez les patients avec rétrécissement aortique sévère symptomatique avec indication de chirurgie non-cardiaque urgente, ou en cas de remplacement valvulaire non faisable, une valvuloplastie percutanée peut être discutée avant la chirurgie, en pont d’un remplacement valvulaire après la chirurgie (grade IIb).
Chez les patients avec insuffisance aortique sévère, symptomatique ou asymptomatique, avec un diamètre télédiastolique > 50 mm, soit 25 mm/m2, ou une FEVG de repos < 50 %, une chirurgie valvulaire est recommandée avant une chirurgie non-cardiaque programmée à risque intermédiaire ou élevée (grade I).
Chez les patients avec rétrécissement mitral modéré à sévère, symptomatique ou avec PAPs > 50 mmHg, une intervention valvulaire (chirurgie ou commissurotomie mitrale percutanée) est recommandée avant une chirurgie non-cardiaque programmée à risque intermédiaire ou élevé (grade I).
Chez les patients avec une insuffisance mitrale sévère primaire, symptomatique ou asymptomatique, avec dysfonction ventriculaire gauche (diamètre télédiastolique > 40 mm et/ou FEVG < 60 %), une intervention valvulaire chirurgicale ou percutanée doit être envisagée, si possible avant une chirurgie non-cardiaque à risque intermédiaire ou élevé (grade IIa).
Chez les patients avec une insuffisance mitrale sévère secondaire restant symptomatique malgré un traitement médical bien conduit, une intervention valvulaire chirurgicale ou percutanée doit être envisagée, si possible avant une chirurgie non-cardiaque à risque intermédiaire ou élevée chez les patients éligibles (grade IIa).
Arythmies et troubles de conduction
Chez les patients avec une arythmie supraventriculaire contrôlée par les médicaments, il est recommandé de poursuivre les anti-arythmiques lors de la période péri-opératoire (grade I).
Une ablation doit être discutée en cas d’arythmie supraventriculaire symptomatique persistante, ou récidivante malgré un traitement médicamenteux optimal, avant une chirurgie non-cardiaque non urgente (grade IIa).
Chez les patients avec tachycardie ventriculaire soutenue monomorphe, récidivante malgré un traitement médical optimal, une procédure d’ablation est recommandée avant une chirurgie non urgente (grade I).
En cas d’extrasystole ventriculaire asymptomatique, il n’est pas recommandé d’introduire de traitement pendant la période péri-opératoire (grade III).
En cas de trouble de conduction nécessitant l’implantation d’un pacemaker, il convient de discuter un report de la chirurgie après cette intervention (grade IIa).
Hypertension pulmonaire
Il est recommandé de poursuivre le traitement de fond d’une hypertension pulmonaire dans la phase péri-opératoire d’une chirurgie non-cardiaque (grade I). Chez ces patients, un monitoring hémodynamique est recommandé au moins dans les 24 heures suivant la chirurgie (grade I).
En cas de progression de l’insuffisance cardiaque droite lors de la période péri-opératoire, il convient d’optimiser la dose de diurétiques et, si nécessaire, d’avoir recours à des analogues de la prostacycline (grade I).
Selon le statut hémodynamique du patient au cours de la période péri-opératoire, il faut discuter l’introduction d’un traitement inodilatateur (dobutamine, milrinone, levosimendan) (grade IIa).
Maladie vasculaire périphérique
Avant une chirurgie d’artériopathie oblitérante des membres inférieurs, ou d’anévrysme de l’aorte abdominale, les patients avec capacité fonctionnelle abaissée, ou avec facteurs de risque ou symptômes significatifs (angor modéré à sévère, insuffisance cardiaque décompensée, valvulopathie, arythmie) doivent bénéficier d’une évaluation cardiaque et d’une optimisation de leur traitement (grade I). En dehors de ces situations, le recours à des examens cardiaques n’est pas recommandé pour ce type de chirurgie (grade III).
Une imagerie carotidienne et cérébrale est recommandée chez les patients avec antécédent d’AVC ou d’AIT au cours des 6 derniers mois avant une chirurgie non-cardiaque (grade I).
3. Complications cardiovasculaires péri-opératoires
Plusieurs complications cardiovasculaires peuvent survenir en péri-opératoire de chirurgie non-cardiaque : infarctus du myocarde et lésion myocardique, insuffisance cardiaque aiguë, maladie veineuse thromboembolique, fibrillation atriale et autres troubles du rythme, AVC, syndrome de Tako-Tsubo.
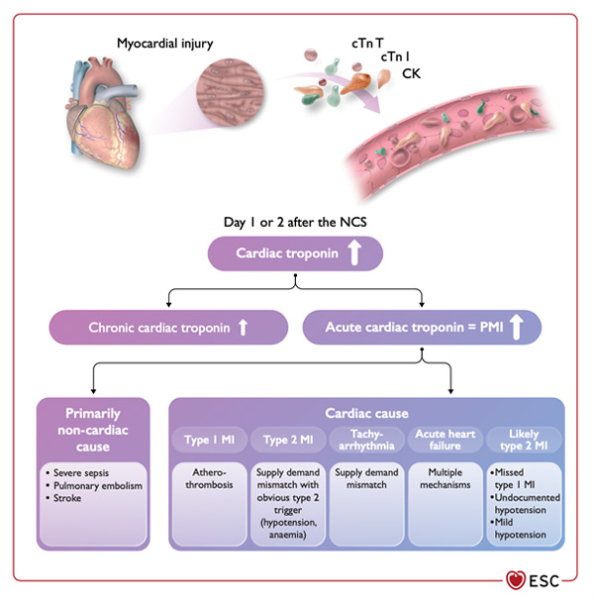
En particulier, la souffrance myocardique péri-opératoire peut avoir plusieurs origines, et un algorithme spécifique de prise en charge est proposé (cf. Figure 10).
Figure 10 - Origines de la souffrance myocardique péri-opératoire
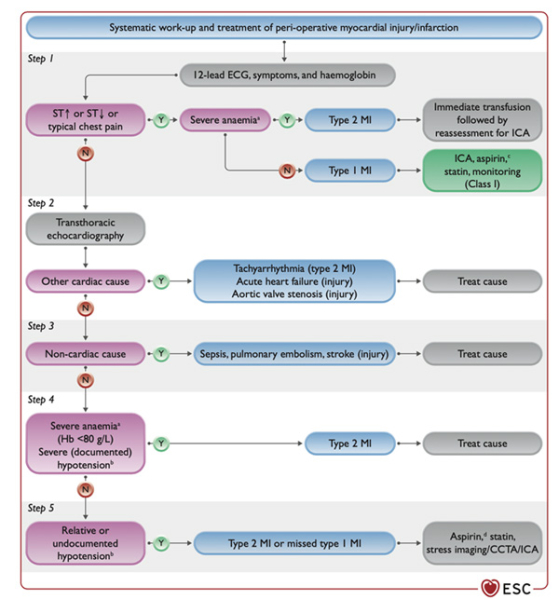
Figure 11 - Bilan et traitement systématiques des lésions/de l'infarctus du myocarde péri-opératoire(s)
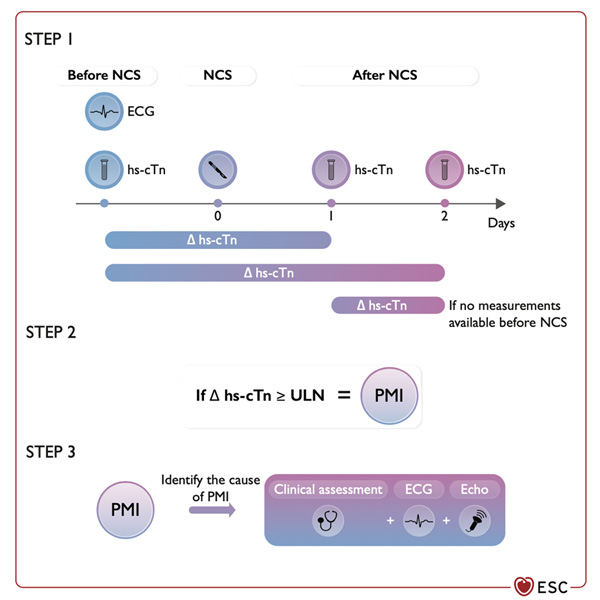
Dans les situations à risque (présence d’une maladie cardiovasculaire ou de facteurs de risque y compris un âge ≥ 65 ans), le dosage de la troponine en pré-opératoire est recommandé afin de le comparer aux valeurs mesurées à 24-48 heures après l’intervention, dans le but de détecter précocement un souffrance myocardique péri-opératoire devant une élévation significative de la troponine.
Figure 12 - Contrôle du dosage de troponine avant, pendant et après la chirurgie non-cardiaque
Il faut également noter que ces recommandations se positionnent en faveur des AOD plutôt que des AVK en cas d’indication d’anticoagulation post-opératoire (fibrillation atriale, embolie pulmonaire).
Concernant la fibrillation atriale post-opératoire, une anticoagulation orale au long cours doit être introduite chez tous les patients avec un risque significatif d’AVC (grade IIb).
L’utilisation en routine des bétabloquants pour prévenir le risque de fibrillation atriale post-opératoire n’est pas recommandée (grade III).
Références
- Smilowitz NR, Gupta N, Guo Y, Beckman JA, Bangalore S, Berger JS. Trends in cardiovascular risk factor and disease prevalence in patients undergoing non-cardiac surgery. Heart 2018;104:1180–6.
- Kristensen SD, Knuuti J, Saraste A, Anker S, Bøtker HE, Hert SD, et al. 2014 ESC/ESA Guidelines on non-cardiac surgery: cardiovascular assessment and management: The Joint Task Force on non-cardiac surgery: cardiovascular assessment and management of the European Society of Cardiology (ESC) and the European Society of Anaesthesiology (ESA). Eur Heart J 2014;35:2383–431.
- 2022 ESC Guidelines on cardiovascular assessment and management of patients undergoing non-cardiac surgery: Developed by the task force for cardiovascular assessment and management of patients undergoing non-cardiac surgery of the European Society of Cardiology (ESC) Endorsed by the European Society of Anaesthesiology and Intensive Care (ESAIC). Eur Heart J 2022;ehac270.
Pour en savoir plus, consultez les guidelines complètes, en langue anglaise, présentées lors de l'ESC 2022 : "2022 ESC Guidelines on cardiovascular assessment and management of patients undergoing non-cardiac surgery"
Toute l'actualité de l'ESC 2022
Ce compte rendu de l'ESC 2022 vous est proposé avec le soutien institutionnel de :
Ce compte rendu d'étude ne reflète pas l'opinion de Cardio Online ou de la SFC, et n'engage pas leur responsabilité.
|