3 minutes de lecture
L’évinacumab : un traitement prometteur dans la prise en charge de l’hypertriglycéridémie sévère
Publié le lundi 17 mai 2021
Auteur :
Clément Bénic
Brest
Relecture :
Pr Martine Gilard
Brest
En direct du congrès de l'ACC 2021
D'après la présentation de Robert S. Rosenson (Tarrytown, États-Unis) : "A Phase 2 Trial Of The Efficacy And Safety Of Evinacumab In Patients With Severe Hypertriglyceridemia".
Contexte
L’hypertriglycéridémie (HTG) sévère (TG > 500 mg/dL) est un facteur de risque de pancréatite aiguë1. Les patients présentant des pancréatites aiguës et porteurs d’une HTG sévère sont plus à risque de présenter de nouvelles crises nécessitant une hospitalisation, avec un pronostic plus défavorable que ceux présentant des pancréatites aiguës sans HTG associées.Il a été démontré que les individus présentant une perte de fonction du gène régulateur de l’angiopoietin-like 3 (ANGPTL3 – jouant un rôle important dans le métabolisme lipidique, agissant par inhibition de la lipoprotéine lipase et de la lipase endothéliale2,3) présentaient un taux de TG et de lipoprotéine pro-athérogène significativement plus bas4,5. L’évinacumab, anticorps monoclonal humain, est un inhibiteur de de l’ANGPTL3 et pourrait donc avoir un rôle intéressant chez les patients porteurs d’une HTG sévère4,5,6.
Méthodes
Il s’agit d’une étude de phase 2, en double aveugle, comparant l’évinacumab contre placebo, avec randomisation en 2/1, ayant inclus 51 patients présentant une HTG sévère avec antécédent d’hospitalisation pour pancréatite aiguë (35 dans le groupe Evinacumab versus 16 patients dans le groupe placebo). L’évinacumab était administré contre placebo sur une période de 12 semaines, puis les deux groupes ont reçu le traitement par évinacumab pendant 12 semaines. Le critère d’évaluation principal était l’évolution du taux de TG à 12 semaines.Les patients ont été divisés en 3 cohortes selon leur génotype :
- HTG avec mutation homozygote sur les gènes APOA5, APOC2, GPIHB1, LMF1 ou LPL : syndrome de chylomicronémie familiale ;
- HTG avec mutation hétérozygote sur ces mêmes gènes avec syndrome de chylomicronémie multifactorielle ;
- HTG sans mutations identifiées sur ces gènes avec syndrome de chylomicronémie multifactorielle.
Résultats
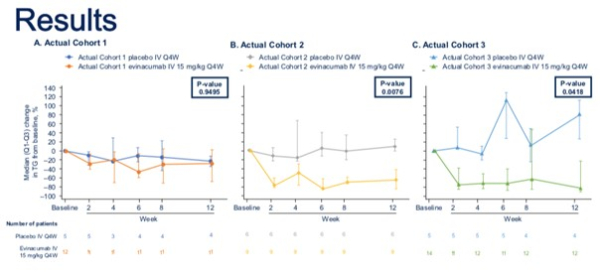
L’évinacumab permet une réduction significative du taux de TG dans le groupe présentant une mutation hétérozygote (-64,8 % versus +9,4 % dans le groupe placebo ; p = 0,0076), ainsi que dans le groupe sans mutations identifiées (-81,7 % versus +80,9 % dans le groupe placebo ; p = 0,0418). Ce bénéfice était maintenu à 24 semaines dans ces deux groupes. En revanche, il n’était pas retrouvé de différences significatives dans le groupe présentant une mutation homozygote (p = 0,9495) (Figure 1).
Figure 1 : Évolution à 12 semaines du taux de TG après traitement par Evinacumab versus placebo, selon le génotype du patientCohorte 1 : Syndrome de chylomicronémie familiale avec mutation homogygoteCohorte 2 : Syndrome de chylomicronémie multifactorielle avec mutation hétérozygoteCohorte 3 : Syndrome de chylomicronémie multifactorielle sans mutations identifiées
Conclusion
L’évinacumab semble être intéressant pour réduire le taux de TG chez les patients présentant une HTG sévère, sans mutations homozygotes identifiées, particulièrement chez les patients ayant déjà présenté une pancréatite aiguë. Des études complémentaires sont nécessaires afin de confirmer ces résultats, notamment dans la prévention secondaire des pancréatites aiguës liées à une HTG sévère.
Références
- Laufs U, Parhofer KG, Ginsberg HN, Hegele RA. Clinical review on triglycerides. Eur Heart J. 1 janv 2020;41(1):99‑109c.
- Musunuru K, Pirruccello JP, Do R, Peloso GM, Guiducci C, Sougnez C, et al. Exome sequencing, ANGPTL3 mutations, and familial combined hypolipidemia. N Engl J Med. 2 déc 2010;363(23):2220‑7.
- Adam RC, Mintah IJ, Alexa-Braun CA, Shihanian LM, Lee JS, Banerjee P, et al. Angiopoietin-like protein 3 governs LDL-cholesterol levels through endothelial lipase-dependent VLDL clearance. J Lipid Res. sept 2020;61(9):1271‑86.
- Dewey FE, Gusarova V, Dunbar RL, O’Dushlaine C, Schurmann C, Gottesman O, et al. Genetic and Pharmacologic Inactivation of ANGPTL3 and Cardiovascular Disease. N Engl J Med. 20 juill 2017;377(3):211‑21.
- Stitziel NO, Khera AV, Wang X, Bierhals AJ, Vourakis AC, Sperry AE, et al. ANGPTL3 Deficiency and Protection Against Coronary Artery Disease. J Am Coll Cardiol. 25 avr 2017;69(16):2054‑63.
- Gaudet D, Gipe DA, Pordy R, Ahmad Z, Cuchel M, Shah PK, et al. ANGPTL3 Inhibition in Homozygous Familial Hypercholesterolemia. N Engl J Med. 20 juill 2017;377(3):296‑7.
Pour consulter le document complet en langue anglaise présenté lors de l'ACC, et accéder aux résultats détaillés, cliquez ici : "Phase 2 Trial of Evinacumab in Patients With Severe Hypertriglyceridemia"
Toute l'actualité de l'ACC 2021
Ce contenu vous est proposé avec le soutien institutionnel de :
Dans la même thématique
Articles les plus lus

Conditions de prescription et de prise en charge des inhibiteurs de PCSK9
Publié le 3 février 2021
RESCUE - Ziltivekimab : un anti-inflammatoire prometteur dans la maladie athéromateuse
Publié le lundi 17 mai 2021
Statines et maladies cardiovasculaires : de la fin de la controverse scientifique à la fin de la polémique ?!
Publié le vendredi 19 mars 2021